- Solutions de retraitement des sondes échographiques
- Solutions de retraitement des sondes échographiques
- Présentation
- Prévention des infections - Quels sont les points à prendre en compte ?
- Prévention des infections - Quels sont les points à prendre en compte ?
- High-Level Disinfection – Combatting HAIs
- Évaluation du risque infectieux lié aux ultrasons
- Automatisation de la désinfection et de la traçabilité
- Garantir l'efficacité - pourquoi le H₂O₂
- Approuvé par des cliniciens du monde entier
- Produits et solutions
- Produits et solutions
- trophon - Protection par conception
- Service et validation
- Apprentissage et soutien
- Apprentissage et soutien
- Lignes directrices et outils
- Académie de Nanosonics
- Solutions de retraitement des endoscopes
- Solutions de retraitement des endoscopes
- Solutions de retraitement des endoscopes
- Solutions de retraitement des endoscopes
- Importance du retraitement
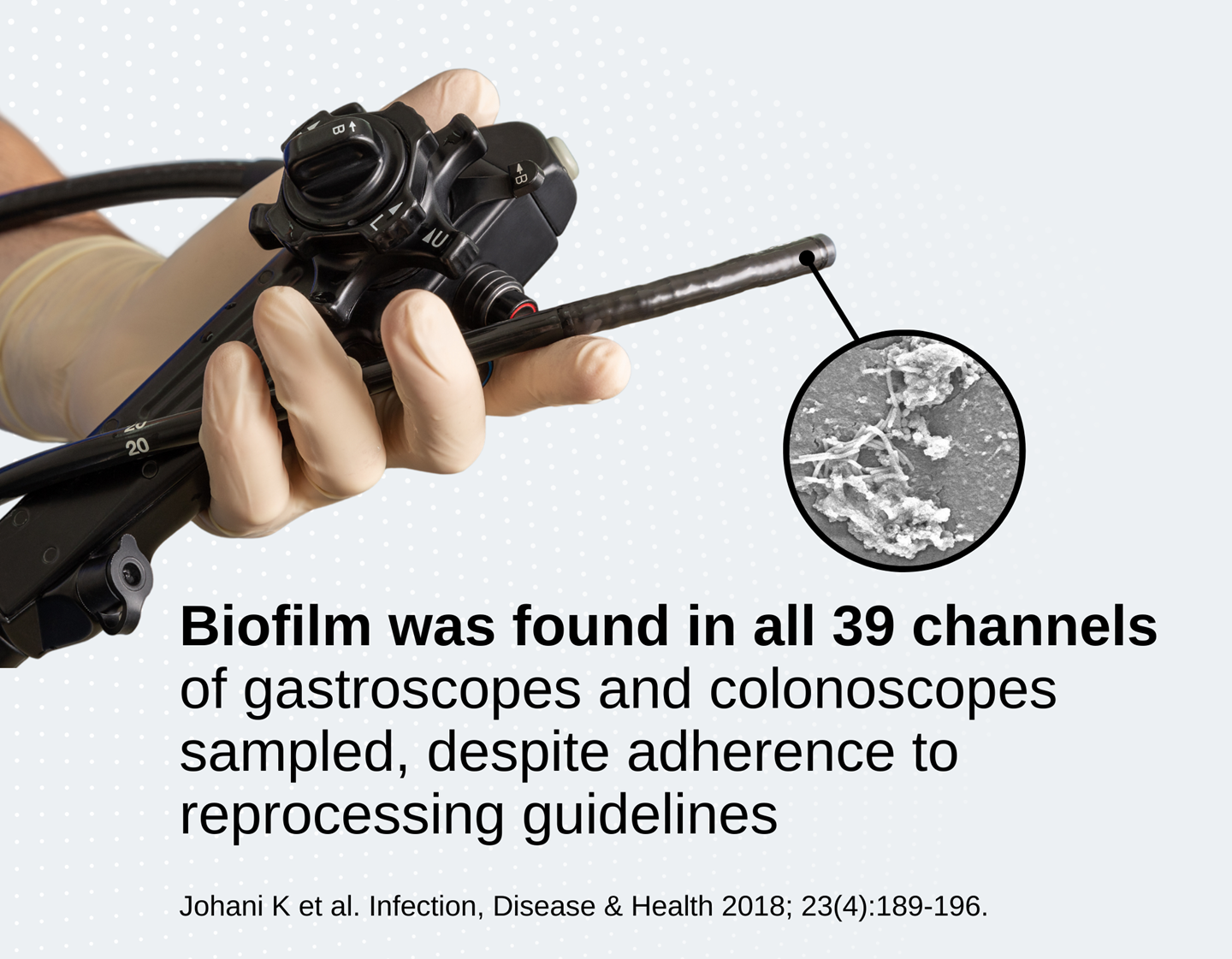
- Biofilm
- Problème lié au nettoyage manuel
- Le prochain étalon-or
- À propos de nous
- À propos de nous
- Contactez-nous
- Contactez-nous
- Contactez
- L'équipe
- Notre histoire
- Investor Centre
- Le Centre
- Académie de Nanosonics
Choose your country and language
You are currently on French